- Introductie
- Hoe werken epigenetische processen
- Over de auteur
- Wetenschappelijke bronnen
“de wetenschap van verandering”
Introductie
In mensen, dieren, planten en elk levend wezen staat alle benodigde informatie dat een cel afleest, om het organisme op te bouwen en te onderhouden en heet DNA. Het wetenschappelijk veld en studie naar ons DNA heet genetica en bestaat sinds het begin van de 19de eeuw. Het heeft de visie op gezondheid en het bestaan flink beïnvloed en toont aan waarom we bijvoorbeeld veel overeenkomst zien tussen ouder en kind.
Het bracht het nature-nurture ‘debat’ voort, waarbij de vraag is welke mate iets veranderbaar is of ‘vaststaat in steen’. Zwart-wit denken is overigens nooit verstandig of een correcte weergave van de realiteit. Met de komst van epigenetica en met name in de laatste twee decennia wordt steeds meer duidelijk en erkend door de wetenschappelijk gemeenschap, dat onze welvaartsziekten niet louter door genen komen, maar meer door hoe we leven en daarmee de epigenetische veranderingen in onze lichaamscellen (13). Zo is een befaamde uitspraak in de gemeenschap dat “genetics loads the gun, but the environment pulls the trigger”. Met andere woorden, zijn welvaartsziekten niet ons lot. Het is niet voor niets dat chronische welvaartsziekten, zoals diabetes type 2, kanker, depressie, hart- en vaatziekte, enzovoorts vrijwel afwezig zijn bij mensen die leven als jager-verzamelaar. Wel kunnen we kwetsbaar zijn voor een eigenschap of ziekte (fenotype).
“genetics loads the gun, but the environment pulls the trigger”
Genetica
Bij de bevruchting is een mens een eencellig wezen (zygote), dat met dat al de benodigde informatie ontvangt van moeder en vader via elk 23 chromosomen. Een zygote dat niet te zien is met het blote oog kan met deze informatie, een samengesteld boek uiteindelijk alles bouwen en groeien tot een ademend, lerend, pratend, voelend en sociaal wezen van ongeveer 41 biljoen cellen. In zo’n megastructuur vol met cellen zit in elke cel dezelfde DNA (exclusief mutaties), als in de ene cel waarmee het begon. Waarom we niet alleen een klodder cellen zijn, maar ook kunnen differentiëren en spiercellen, zenuwcellen of botcellen kunnen maken wordt bepaald door epigenetica. Epigenetica bepaald wat er in het boek wordt afgelezen. Feiten over genetica opgesomd:
– Cellen zijn fundamentele ‘werkeenheden’ van ieder mens en we bestaan uit circa 41 biljoen (41.000 miljard) Alle instructies die nodig zijn om hun activiteiten te sturen, bevinden zich in het chemische deoxyribonucleïnezuur, ook bekend als DNA.
– DNA van mensen bestaat uit ongeveer 3 miljard nucleotidebasen. Er zijn vier fundamentele soorten basen die DNA omvatten – adenine, cytosine, guanine en thymine, gewoonlijk afgekort als respectievelijk A, C, G en T.
– Interessant genoeg is onze DNA grotendeels (99%) vergelijkbaar met die van een chimpansee.
– Binnen de 3 miljard basen zijn er ongeveer 20.000 genen. Genen zijn specifieke sequenties van basen die instructies geven over het maken van belangrijke eiwitten – complexe moleculen die verschillende biologische acties in gang zetten om levensfuncties uit te voeren.
Epigenetica
Epigenetica bepaalt en gaat over welke genen worden afgelezen en welke eiwitten worden opgebouwd. Dat we genetisch alleen al voor 99% lijken op chimpansees en 99,9% op elkaar (mens tussen mens) geeft al een weer hoe de omstandigheden de verschillen ‘moeten’ verklaren.
Het DNA, genotype of analogisch verwoord ‘het boek met informatie’ dat we meedragen, is in principe niet veranderbaar (uitgezonderd mutaties en d.m.v. gentechnologie). Welke genen en pagina’s uit het boek worden afgelezen (gen-expressie) bepaalden welke eiwitten worden aangemaakt en dat bepaalt uiteindelijk alle functies (fenoytypen) in de mens, zoals lengte, spierkracht, gedrag, hartslag en bewustzijn. Het fenotype ofwel hoe we er aan de ‘buitenkant uitzien’ (natuurlijk ook binnenkant) is daarmee beïnvloedbaar. Enkele feiten over epigenetica opgesomd:
– Epigenetica controleert genen: Epigenetica bepaalt de specialisatie van een cel (bijv. huidcel, bloedcel, haarcel, levercellen, enzovoorts)
– Omgevingsprikkels kunnen er ook voor zorgen dat genen worden uit- of ingeschakeld.
– Epigenetica is overal: Wat je eet, waar je woont, met wie je omgaat, wanneer je slaapt, hoe je traint, zelfs ouder worden – dit alles kan uiteindelijk chemische modificaties veroorzaken rond de genen die die genen in de loop van de tijd aan of uit zullen zetten.
– Epigenetica maakt ons uniek. Tweelingen zijn genetisch hetzelfde, maar toch anders en krijgen niet dezelfde ziekten. Waarom haten sommigen van ons de smaak van champignons of aubergines? Waarom zijn sommigen van ons socialer dan anderen? De verschillende combinaties van genen die aan of uit worden gezet, maken ieder van ons uniek.
– Er is duidelijk bewijs epigenetische veranderingen zelfs worden overgeërfd.
– Epigenetica is omkeerbaar. Met meer dan 20.000 genen, kan het resultaat zijn van het in- of uitschakelen van de verschillende combinaties van genen enorm zijn.
Hoe werken epigenetische processen
Wat wordt afgelezen in onze boek met genen staat dus onder invloed van epigentische processen. Deze processen betreffen methylatie, acetylatie en niet coderend RNA. Deze geven veranderingen die dus ook weer omkeerbaar zijn en veranderen de DNA-streng zelf niet, maar wel de expressie van een gen. Gen-expressie verwijst naar het wel of niet en de mate van uiting komen van een gen. Wanneer een gen tot uiting komt, wordt een corresponderend eiwit geproduceerd. De eiwitten die gemaakt worden bepalen uiteindelijk alle functies (fenoytypen) in de mens, zoals lengte, spierkracht, gedrag, hartslag en bewustzijn. Deze epigenetische processen treden op na seconden, dagen en houden maanden tot jaren aan.
DNA methylering en demethylering
DNA methylatie werkt door een methylgroep aan het DNA toe te voegen. Meestal wordt deze groep toegevoegd aan specifieke plaatsen op het DNA, waar het de eiwitten blokkeert die zich aan het DNA hechten om het gen te lezen. Deze methylgroep kan worden verwijderd via een proces dat demethylering wordt genoemd. Doorgaans zet methylering genen uit en zet demethylering genen aan.
Histon acetylering en deacetylering
DNA wikkelt zich rond eiwitten die histonen worden genoemd. DNA dat strak om histonen is gewikkeld, is niet toegankelijk voor eiwitten die het gen lezen. Sommige genen zijn rond histonen gewikkeld en worden uit gezet, terwijl sommige genen niet rond histonen zijn gewikkeld en aan zijn gezet. Bepaalde moleculen kunnen worden toegevoegd aan of verwijderd van histonen en wijzigen of een gen wordt uitgepakt of verpakt; aan of uit.
Niet-coderend RNA
Je DNA wordt gebruikt als instructies voor het maken van coderend en niet-coderend RNA. Coderend RNA wordt gebruikt om eiwitten te maken. Niet-coderend RNA helpt de genexpressie onder controle te houden door zich te hechten aan coderend RNA, samen met bepaalde eiwitten, om het coderende RNA af te breken, zodat het niet kan worden gebruikt om eiwitten te maken. Niet-coderend RNA kan ook eiwitten rekruteren om histonen te modificeren om genen aan of uit te zetten.
Epigenetica en ontwikkeling
Epigenetische veranderingen beginnen voordat een individu wordt geboren. Alle cellen hebben dezelfde genen, maar zien er anders uit en gedragen zich anders. Terwijl een mens groeit en zich ontwikkelt, helpt epigenetica te bepalen welke functie een cel zal hebben, bijvoorbeeld of het een hartcel, zenuwcel of huidcel wordt.
Je spiercellen en zenuwcellen hebben hetzelfde DNA maar werken anders. Een zenuwcel transporteert informatie naar andere cellen in uw lichaam. Een spiercel heeft een structuur die helpt bij het bewegen van uw lichaam. Epigenetica stelt de spiercel in staat om genen aan te zetten om eiwitten belangrijk te maken voor zijn werk en om genen uit te schakelen die belangrijk zijn voor het werk van een zenuwcel.
Epigenetica en leeftijd
Epigenetica verandert gedurende het gehele leven. De epigenetische programmering zal bij de geboorte zeker niet dezelfde zijn als tijdens de kindertijd of volwassenheid. Epigenetica verandert dus naarmate een mens ouder wordt, zowel als onderdeel van normale ontwikkeling en veroudering als reactie op omgeving en leefstijl.
Voorbeeld: studie van pasgeboren vs. 26-jarige vs. 103-jarige
DNA-methylatie op miljoenen DNA-locaties werd gemeten bij een pasgeborene, 26-jarige en 103-jarige. Het niveau van DNA-methylatie neemt af met de leeftijd. Een pasgeborene had de hoogste DNA-methylering, de 103-jarige had de laagste DNA-methylatie en de 26-jarige had een DNA-methyleringsniveau tussen de pasgeborene en de 103-jarige (1).
Epigenetica en omkeerbaarheid
Epigenetische veranderingen zijn dikwijls niet permanent. Vele epigenetische veranderingen kunnen worden toegevoegd of verwijderd als reactie op veranderingen in gedrag of omgeving.
Voorbeeld: rokers vs. niet-rokers vs. ex-rokers
Roken kan leiden tot epigenetische veranderingen. Op bepaalde delen van het AHRR-gen hebben rokers bijvoorbeeld minder DNA-methylering dan niet-rokers. Het verschil is groter voor zware rokers en langdurig rokers. Na het stoppen met roken, kunnen ex-rokers een verhoogde DNA-methylatie krijgen bij dit gen. Uiteindelijk kunnen ze niveaus bereiken die vergelijkbaar zijn met die van niet-rokers. In sommige gevallen kan dit binnen een jaar gebeuren, maar de tijdsduur hangt af van hoe lang en hoeveel iemand rookte voordat hij stopte (2).
Epigenetica in relatie met bepaalde ziekten
Epigenetische veranderingen kunnen gezondheid op verschillende manieren beïnvloeden: Pathogenen kunnen epigenetica veranderen om het immuunsysteem te verzwakken. Dit helpt de pathogeen te overleven.
Voorbeeld: Mycobacterium tuberculosis
Mycobacterium tuberculosis veroorzaakt tuberculose. Infecties met deze ziektekiemen kunnen veranderingen in histonen veroorzaken in sommige van de immuuncellen, waardoor het IL-12B-gen wordt uitgeschakeld. Als het IL-12B-gen uitgeschakeld wordt, verzwakt het immuunsysteem en kan de Mycobacterium tuberculosis makkelijker overleven (3).
Kanker
Bepaalde genetische aanleg, alsmede bepaalde epigenetische veranderingen verhogen het risico op kanker. Bij een mutatie op het BRCA1-gen waardoor het niet goed werkt, is de kans groter op borst- en andere vormen van kanker. Daarbij verhoogt verhoogd DNA-methylatie dat resulteert in verminderde BRCA1-genexpressie het risico op borst- en andere kankers (4). Hoewel kankercellen een verhoogde DNA-methylatie hebben bij bepaalde genen, zijn de algehele DNA-methyleringsniveaus lager in kankercellen vergeleken met normale cellen. Verschillende soorten kanker die op elkaar lijken, kunnen verschillende DNA-methylatiepatronen hebben. Epigenetica kan worden gebruikt om te helpen bepalen welk type kanker iemand heeft of kan helpen om eerder moeilijk te detecteren kankers te vinden. Epigenetica alleen kan kanker niet diagnosticeren.
Voorbeeld: colorectale kanker
Colorectale kankers hebben een verhoogde methylering bij het SEPT9-gen. Sommige commerciële epigenetische tests voor colorectale kanker kijken naar DNA-methyleringsniveaus op het SEPT9-gen. Bij gebruik in combinatie met andere diagnostische screeningstests kunnen deze op epigenetische basis gebaseerde tests helpen om kanker vroegtijdig te vinden (5,6).
Obesitas
Voeding, bewegingsarmoede, chemicaliën en stress zorgen voor epigenetische veranderingen, uiteindelijk leidend tot obesitas (zie illustratie) (13).
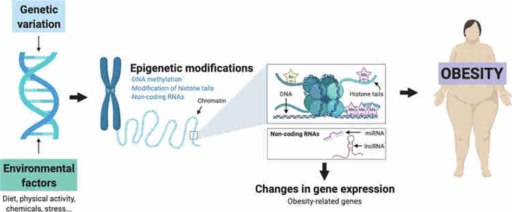
Illustratie: “The role of epigenetics in the development of obesity” (13).
Zwangerschap en epigenetische veranderingen bij het kind
De omgeving en het gedrag van een zwangere vrouw tijdens de zwangerschap, bijvoorbeeld of ze gezond eet, kan de epigenetica van de baby veranderen. Sommige van deze veranderingen kunnen tientallen jaren aanhouden en kunnen ervoor zorgen dat het kind meer kans heeft op het krijgen van bepaalde ziekten.
Voorbeeld: De Nederlandse honger winter (1944-1945)
Mensen van wie de moeders tijdens de hongersnood zwanger waren, hadden meer kans om bepaalde ziekten te ontwikkelen, zoals hartaandoeningen, schizofrenie en diabetes type 2 (7). Ongeveer 60 jaar na de hongersnood keken onderzoekers naar methyleringsniveaus bij mensen van wie de moeders tijdens de hongersnood zwanger van hen waren. Deze mensen hadden een verhoogde methylering bij sommige genen en een verminderde methylering bij andere genen in vergelijking met hun broers en zussen die vóór hun geboorte niet aan hongersnood waren blootgesteld (8,9,10). Deze verschillen in methylering zouden kunnen helpen verklaren waarom deze mensen een verhoogde kans hadden op bepaalde ziekten later in hun leven (7,10,11,12).
Over de auteur

Drs. Sjoerd Knobben, is psycholoog en klinische PsychoNeuroImmunologische therapeut, trainer in mindfulness, martial arts (o.a. Kung Fu) en voorzitter bestuur kPNI.nl. Alles komt samen in zijn praktijk voor zelf-actualisatie en gezondheid, Upotential.
Wetenschappelijke bronnen
(1). Heyn H, Li N, Ferreira H, et al., Distinct DNA methylomes of newborns and centenariansexternal icon. Proc Natl Acad Sci U S A 2012; 109:10522-7
(2). McCartney D, Stevenson A, Hillary R, et al., Epigenetic signatures of starting and stopping smokingexternal icon. EBioMedicine 2018; 37:214-220
(3). Chandran A, Antony C, Jose L, et al., Mycobacterium Tuberculosis Infection Induces HDAC1-Medicated Suppression of IL-12B Gene Expression in Macrophagesexternal icon. Front Cell Infect Microbiol 2015; 5:90.
(4).Tang Q, Cheng J, Cao X, et al., Blood-based DNA methylation as biomarker for breast cancer: a systematic reviewexternal icon. Clin Epigenetics 2016; 8: 115.
(5). Johnson D, Barclay R, Mergener K, et al., Plasma Septin9 Versus Fecal Immunochemical Testing for Colorectal Cancer Screening: A Prospective Multicenter Studyexternal icon. PLoS One 2014; 9:e98238.
(6). Food and Drug Administration. Epi proColonpdf iconexternal icon. 2016 [accessed 29 June 2020].
(7). Roseboom T., Epidemiological evidence for the developmental origins of health and disease: effects of prenatal undernutrition in humansexternal icon. J Endocrinol 2019. 242:T135-T144
(8). Heijmans B, Tobi E, Stein A, et al., Persistent epigenetic differences associated with prenatal exposure to famine in humansexternal icon. Proc Natl Acad Sci U S A 2008; 105: 17046-17049.
(9). Tobi E, Lumey L, Talens R, et al., DNA Methylation Differences After Exposure to Prenatal Famine Are Common and Timing- And Sex- Specificexternal icon. Hum Mol Genet 2009; 18:4046-53.
(10). Tobi E, Slieker R, Luijk R, et al., DNA methylation as a mediator of the association between prenatal adversity and risk factors for metabolic disease in adulthoodexternal icon. Sci Adv 2018; 4:eaao4364.
(11). Dayeh T, Tuomi T, Almgren P, et al., DNA Methylation of Loci Within ABCG1 and PHOSPHO1 in Blood DNA is Associated With Future Type 2 Diabetes Riskexternal icon. Epigenetics 2016; 7: 482-8.
(12). Pidsley R, Dempster E, Troakes C, et al., Epigenetic and genetic variation at the IGF2/H19 imprinting control region on 11p15.5 is associated with cerebellum weightexternal icon. Epigenetics 2012; 7:155-163.
(13). A. Obri, D. Serra, L. Herrero, P. Mera, The role of epigenetics in the development of obesity, Biochemical Pharmacology (2020), doi: https://doi.org/10.1016/j.bcp.2020.113973
(14). Münzel, T., Sørensen, M., Lelieveld, J., Hahad, O., Al-Kindi, S., Nieuwenhuijsen, M., Giles-Corti, B., Daiber, A., & Rajagopalan, S. (2021). Heart healthy cities: genetics loads the gun but the environment pulls the trigger. European heart journal, 42(25), 2422–2438. https://doi.org/10.1093/eurheartj/ehab235





