“It’s all about energy”
–Nature
Energieverdeling
Geassocieerde symptomen:
Alcoholintolerantie
Futloosheid
Winderigheid
Bloedstollingsstoornissen
Hoge bloedruk
Uitputting
Eetstoornissen
Koude handen of voeten (hypothermie)
Spierafbraak
Laaggradige ontstekingen
Peesklachten (tendinitis)
Stemmingsstoornissen
Overgewicht
Geassocieerde ziektebeelden:
Auto-immuunziekten
Diabetes melitus type 2 en insuline resistentie
Metabool syndroom
Multiple organische klachten
Neuro-degeneratieve aandoeningen
Osteoporose
Hypothreoïde (traag werkende schildklier)
Slijmbeursontsteking (bursitis)
Tenniselleboog (epicondylitis)
Energie en het leven
De uitspraak “it’s all about energy” is de rode draad in de natuur en staat dus centraal in het functioneren van een mens. Van de circa 46 biljoen (=46.000.000.000.000) cellen in ons lichaam heeft iedere afzonderlijke cel energie nodig. Maar wat is energie precies en wat gebeurt er als energie ontbreekt. We zullen eerst het werkinsmechanisme energieverdeling onder de loep moeten nemen willen we verzamelingen van cellen zoals weefsels, organen en systemen kunnen aanpakken. Voldoende energie op de juiste plaats is de voorwaarde voor het optimaal kunnen functioneren van lichaam en psyche. Voedsel is er in onze streken genoeg, en daarom gaat het hier vooral om hoe energie optimaal opgenomen, sneller opgebouw, beter vastgehouden en op de juiste manier verdeeld kan worden.
Energie is ATP
Adenosinetrifosfaat (ATP) is de universele energiebron die de mens gebruikt als energiebron, die we idealiter uit de verbranding van vetten, maar ook uit eiwitten en koolhydraten halen. De citroenzuurcyclus in de energiecentrale van de cellen (de mitochondrieën) is de oudst bekende enzymafhankelijke stofwisselingsroute voor de productie van ATP. Net als alle andere levende wezen op aarde heeft de mens een ruststofwisseling (BMR=basale metabolic rate) dat, zoals de definitie al aangeeft, het noodzakelijke aantal calorieën waarmee lichaamstemperatuur en de primaire levensprocessen in rust, in stand kan worden gehouden. Dat is tegenwoordig voor een man 1500 kcal en voor een vrouw 1380 kcal. Dit is gemiddeld 200 kcal minder vergeleken met volkeren die nu nog als vissers, jagers of verzamelaars leven, wat waarschijnlijk verband houdt met hun grotere spiermassa.
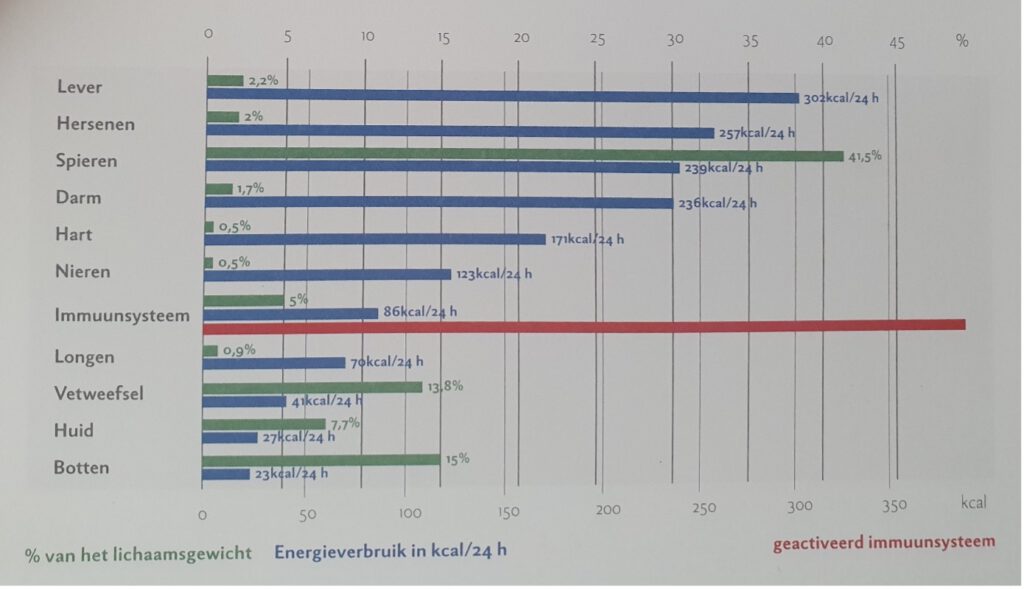
Het basale energieverbruik hangt hoofdzakelijk af van de omvang en de activiteit van de hersenen, de inwendige organen en de spiermassa. In onderstaande afbeelding zien we het energieverbruik in rust en het gewicht per orgaan als percentage van het lichaamsgewicht staat weergegeven. Opvallend is dat 69% van de energie in rust wordt verbruikt door de interne organen en waarvan het grootste gedeelte in warmte wordt omgezet om een stabiele lichaamstemperatuur van 36,5 graden celcius in stand te kunnen houden (1). Deze verdeling verandert duidelijk zodra bijv. De spieren en de longen of het immuunsysteem geactiveerd worden (2).
Energie en spieren
Een belangrijke verandering in de afgelopen 200 jaar is de afname van lichamelijk aciviteit bij mensen, en daarmee samenhangend, hun geringere spiermassa. Uit onderzoek in de afgelopen jaren is gebleken dat het spierstelsel veel meer is dan alleen een bewegingsorgaan. Het is een van de belangrijkse metabole (stofwisseling), endocriene (hormonen) en immunologische (afweer) organen van het menselijke lichaam. Onze spiermassa is zelfs zo belangrijk dat de hoeveelheid een significante invloed heeft op onze levensverwachting (4,5). Herstel van een bepaalde hoeveelheid spiermassa samen met herstel van de energieverdeling naar ‘verwaarloosde’ organen, zorgt voor vermindering van de inflammatoire activiteit van het immuunsysteem, waardoor energie gespaard wordt.
Inflammatoire activiteit en energieproblemen
Mensen verliezen hun spierweefsel niet alleen door inactivitieit, maar ook door gebrekkig voeding, en vooral door een vaak chronische activiteit van het immuunsysteem (6). Het metabool syndroom veroorzaakt ophoping en groei van vetweefsel met ontstekingsactiviteit, waardoor het immuunsysteem chronisch inflammatoir actief wordt. Uit wetenschappelijke gegevens blijkt dat tot wel 95% van de alle mensen in de geindustrialiseerde landen door de chronische (laaggradige) ontstekingsactiviteit van het immuunsysteem getroffen wordt (7).
De langdurige verhoogde inflammatoire werking van het immuunsysteem kost zeer veel energie, waardoor andere organen in gevaar kunnen komen (8). Een mogelijk gevolg daarvan is orgaanfalen en eventueel zelfs de dood. De enige (evolutionaire) oplossing daarvoor is ‘overwintering’ van de interne organen – organen worden als het ware in de spaarstand gezet – waarmee het basale energieverbruik afneemt. Het is het evolutionaire programma van ‘vandaag overleven en morgen zien we wel’. Het immuunsysteem is zelfs in staat om weefsel dat niet direct nodig is om te overleven af te breken om de noodzakelijke energie vrij te maken voor het immuunsysteem.
De twee belangrijkse kandidaten voor de afbraak van weefsel in het voordeel van het immuunsysteem zijn het bindweefsel en daarna het spierweefsel. Zo kan een belangrijke spier als het middenrif (diafragma) tot wel 30% worden afgebroken. Dit is de verklaring, en dus geen toeval, dat mensen die langdurige stress ervaren pijnklachten krijgen op hun borst door kleine spierscheurtjes. Dit ontstaat sneller als spierweefsel kwetsbaar wordt door energietekort en afbraak.
Waarom breekt het immuunsysteem het lichaam af?
Het antwoord ligt in de evolutie van het immuunsysteem. Dit systeem heeft als belangrijkste taak het lichaam te beschermen tegen allerlei indringen waaronder het influenzavirus. Als dit virus griep veroorzaakt heeft de patient geen eetlust meer, is moe, slaapt veel en heeft flinke koorts. Nadat het virus met succes bestreden is krijgt de genezen patient een enorme honger en dorst, om zodoende het evenwicht weer te herstellen. Dit voorbeeld illustreert een paar belangrijke principes:
- Zodrag het immuunsysteem geactiveerd wordt, ontstaat een gevoel van algehele malaise en ziektegedrag, waaronder weigeren van eten, veel slapen en zich terugtrekken.
- Tijdens een infectie worden nauwelijks voedingsstoffen opgenomen.
Het verminderen van de eetlust lijkt op het eerste gezicht contraproductief gezien het feit dat een actief immuunsysteem veel meer energie verbruikt dan een immuunsysteem in rust – van 370 kcal per dag naar wel 2000 kcal bij een bloedvergiftiging (9). Niets is minder waar: De eetlustvermindering is in eerste instantie bedoeld om er voor te zorgen dat er niet nog meer ziekteverwekkers (pathogenen) kunnen binnendringen. Voordat de ijskast bestond waren deze ziekteverwekkers zonder twijfel (meer) aanwezig in voedsel.
De tweede reden is dat het te lang zou duren om energie uit voedsel te halen, en dat het ook niet zeker is hoeveel het immuunsyseem dan werkelijk uit die voeding zou krijgen. Aangezien een falend afweersysteem onze dood zou kunnen betekenen, wordt onder alle omstandigheden gezorgd voor een goed functionerende energievoorziening van het immuunsysteem. Het immuunsysteem dwingt het lichaam tot een metabolische schakeling en gaat anders energie produceren. Wanneer het immuunsysteem niet actief is, wordt de energie (ATP) namelijk in de energiecentrales van het de cellen (de mitochrondriën) geproduceerd. Wanneer ons immuunsysteem geactiveerd is, maakt het gebruik van de honderdmaal snellere, zogenaamde aerobe (met zuurstof) glycolyse (10). Tijdens aerobe glycolyse wordt glucose voor een groot deel gefermenteerd in melkzuur, aminozuren, vetmoleculen en zelfs nucleotiden, terwijl een klein deel van de aanwezige glucose in pyruvaat en daarmee in energie (ATP) wordt omgezet. De geproduceerde macromoleculen kunnen nu gebruikt worden om nieuwe immuuncellen aan te maken en te voeden.
Hoe een langdurige (laaggradige) ontsteking energieproblemen veroorzaakt
Wegens het feit dat onsteking een verminderde opname en bovendien grootverbruiker is van energie en bepaalde moleculen zoals aminozuren, ontstaat er in toenemende mate het risico op tekorten.
De gluconeogenese uit aminozuren kan zo groot zijn dat het immuunsysteem de omzet van eiwit verdrievoudigt. Er zijn 19 aminozuren die omgezet kunnen worden in energie (glucose), en afhankelijk van de aminozuren die gebruikt worden om in immuunenergie omgezet te worden, kunnen bepaalde syndromen of aandoeningen ontstaan (6-8).
Een veelkomend voorbeeld hiervan is de ontwikkeling van een depressie. Mensen met een depressie hebben dan een laaggradige ontsteking en verbruiken grote hoeveelheden van het aminozuur tryptofaan (als voorloper van glucose). Serotonine is een neurotransmitter die in de hersenen wordt gebruikt voor prikkeloverdracht. Tryptofaan wordt gebruikt voor de aanmaak van serotonine. Doordat tryptofaan nu wordt gebruikt voor de aanmaak van glucose kan er een stoornis ontstaan in de serotoninehuishouding. Een serotoninetekort in het brein is onderdeel van het ziektebeeld depressie. De strategie die het immuunsysteem kiest om aminozuren te gebruiken voor de energievoorziening van het immuunsysteem kan worden gezien als een stap in de ontwikkeling van een ziektebeeld. Welk aminozuurstrategie is gebaseerd op de epigenetische (omkeerbare erfelijke verandering) gevoeligheid van een mens. Deze stap leidt tot de ontwikkeling van een aandoening (‘de ziektefilm’), die hoort bij een bepaalde persoonlijkheid: de persoonlijkheid kiest de ziekte.
Veel informatie uit deze tekst is afkomst uit “Word weer mens. De terugkeer van homo sapiens” door dr. L. Pruimboom. Vind in dit boek verdere informatie betreffende dit onderwerp.
Over de auteur

Drs. Sjoerd Knobben, ‘eeuwige student van het leven’ is psycholoog en klinische PsychoNeuroImmunologische therapeut, docent bij PNI europe, trainer in mindfulness, martial arts (o.a. kung fu) en voorzitter bestuur kPNI.nl. Alles komt samen in zijn praktijk voor zelf-actualisatie en gezondheid, genaamd Upotential.
Upotential.nl kpni.nl cpnieurope.nl ivmv.org
Bronnen
(1) Pruimboom L. (2011). Physical inactivity is a disease synonymous for a non-permissive brain disorder. Medical hypotheses, 77(5), 708–713. https://doi.org/10.1016/j.mehy.2011.07.022
(2) Lochmiller, R.L. and Deerenberg, C. (2000), Trade-offs in evolutionary immunology: just what is the cost of immunity?. Oikos, 88: 87-98. https://doi.org/10.1034/j.1600-0706.2000.880110.x
(3) Pruimboom, L. & Reiheis, D. (2018) Word weer mens. De terugkeer van homo sapiens. Plumtree Editorial. ISBN 978-90-826415-3-0
(4) Evans, D. S., Kapahi, P., Hsueh, W. C., & Kockel, L. (2011). TOR signaling never gets old: aging, longevity and TORC1 activity. Ageing research reviews, 10(2), 225–237. https://doi.org/10.1016/j.arr.2010.04.001
(5) Mador M. J. (2002). Muscle mass, not body weight, predicts outcome in patients with chronic obstructive pulmonary disease. American journal of respiratory and critical care medicine, 166(6), 787–789. https://doi.org/10.1164/rccm.2206003
(6) Straub R. H. (2011). Concepts of evolutionary medicine and energy regulation contribute to the etiology of systemic chronic inflammatory diseases. Brain, behavior, and immunity, 25(1), 1–5. https://doi.org/10.1016/j.bbi.2010.08.002
(7) Ruiz-Núñez, B., Pruimboom, L., Dijck-Brouwer, D. A., & Muskiet, F. A. (2013). Lifestyle and nutritional imbalances associated with Western diseases: causes and consequences of chronic systemic low-grade inflammation in an evolutionary context. The Journal of nutritional biochemistry, 24(7), 1183–1201. https://doi.org/10.1016/j.jnutbio.2013.02.009
(8) Nalam, R. L., Pletcher, S. D., & Matzuk, M. M. (2008). Appetite for reproduction: dietary restriction, aging and the mammalian gonad. Journal of biology, 7(7), 23. https://doi.org/10.1186/jbiol84
(9) Dantzer, R., & Kelley, K. W. (2007). Twenty years of research on cytokine-induced sickness behavior. Brain, behavior, and immunity, 21(2), 153–160. https://doi.org/10.1016/j.bbi.2006.09.006
(10) Pfeiffer, M., von Bauer, R., & Nawroth, P. P. (2011). The new puzzle about the treatment of type 2 diabetes after the ACCORD and Da Qing studies. Langenbeck’s archives of surgery, 396(7), 941–947. https://doi.org/10.1007/s00423-011-0781-z





